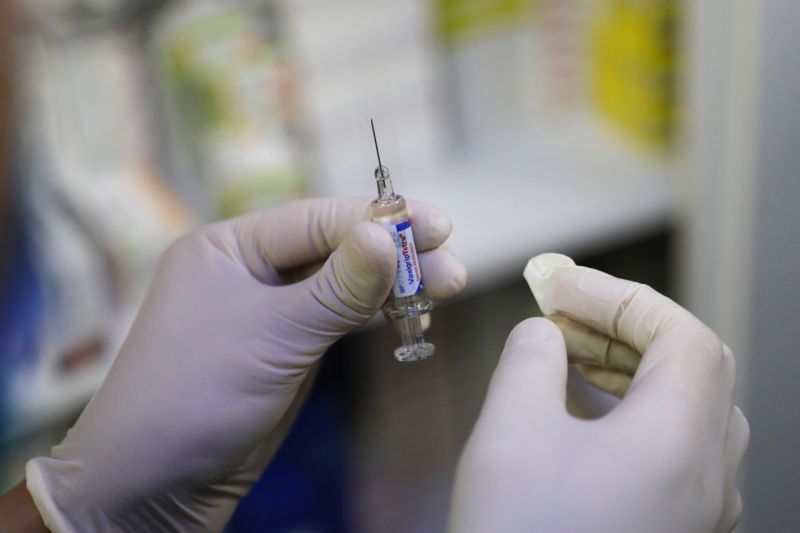
(中央社華盛頓23日綜合外電報導)兩款試驗中的新型冠狀病毒疫苗因受試者出現狀況而喊卡,在確認問題與疫苗本身無關後,美國核准這兩款疫苗恢復在美臨床試驗。巴西監管當局則特許進口北京科興研發的疫苗。
法新社報導,2019冠狀病毒疾病(COVID-19)已在美國奪走超過22萬3000條人命,也成為美國總統大選中現任共和黨籍總統川普(Donald Trump)與民主黨籍對手拜登(Joe Biden)互相攻防的頭號議題。
英國製藥阿斯特捷利康公司(AstraZeneca)宣布,與牛津大學(University of Oxford)共同研發的疫苗已在美國恢復臨床試驗。該公司疫苗9月6日在英國的試驗出現一名受試者罹患神經系統疾病,導致試驗喊卡。但英國很快就恢復試驗,接著南非、巴西與日本也陸續恢復,只剩美國未放行。
阿斯特捷利康公司說:「繼其他國家於近幾週恢復臨床試驗後,美國食品暨藥物管理局(FDA)今天批准在美國重新展開試驗。」業者表示希望疫苗試驗結果能在年底出爐。
全球展開研製疫苗競賽,阿斯特捷利康與牛津大學合作研發的疫苗,被認為是目前最有可能搶先問世的疫苗之一。全球迄今已有110萬人死於COVID-19。
與此同時,嬌生集團(Johnson & Johnson)10月12日因一名受試者出現不良反應後暫停試驗,今天也宣布準備恢復招募受試者。
美國媒體報導,嬌生集團首席科學官史托佛(PaulStoffels)表示,試驗暫停期間除公司內部的檢查機制外,還有3個獨立的外部醫學顧問分析問題細節,「沒有發現證據顯示問題與疫苗有關」。
史托佛說,美國的試驗應能在26日前恢復進行,他以隱私為由不透露先前試驗出現副作用的細節,但據華盛頓郵報披露,先前的問題是一名受試者中風。
美國衛生及公共服務部(HHS)官員曼戈(PaulMango)說,他預期美國今年底前就能取得足夠疫苗供「最脆弱」族群,明年1月底前所有年長者都能施打,到明年3、4月底前全體美國民眾都能打得到疫苗。
另一方面,雖然巴西總統波索納洛(JairBolsonaro)本週稍早還宣布不會採購中國北京科興生物公司(Sinovac Biotech)的疫苗Coronavac,但巴西國家衛生監測局(Anvisa)今天中午發表聲明,特許北京科興的研究夥伴、聖保羅的布坦坦研究所(Instituto Butantan)進口600萬劑Coronavac疫苗供第3期臨床試驗之用。
巴西國內為中製疫苗引發爭執,總統嫌棄中製疫苗,但包括聖保羅州長多利亞(Joao Doria)在內的地方首長,以及國會下議院議長梅雅(Rodrigo Maia),都與總統唱反調;多利亞說阻撓北京科興疫苗在巴西的試驗根本就是「犯罪」,痛批總統把疫苗政治化。(譯者:陳怡君/核稿:陳亦偉)1091024
我是廣告 請繼續往下閱讀
英國製藥阿斯特捷利康公司(AstraZeneca)宣布,與牛津大學(University of Oxford)共同研發的疫苗已在美國恢復臨床試驗。該公司疫苗9月6日在英國的試驗出現一名受試者罹患神經系統疾病,導致試驗喊卡。但英國很快就恢復試驗,接著南非、巴西與日本也陸續恢復,只剩美國未放行。
阿斯特捷利康公司說:「繼其他國家於近幾週恢復臨床試驗後,美國食品暨藥物管理局(FDA)今天批准在美國重新展開試驗。」業者表示希望疫苗試驗結果能在年底出爐。
全球展開研製疫苗競賽,阿斯特捷利康與牛津大學合作研發的疫苗,被認為是目前最有可能搶先問世的疫苗之一。全球迄今已有110萬人死於COVID-19。
與此同時,嬌生集團(Johnson & Johnson)10月12日因一名受試者出現不良反應後暫停試驗,今天也宣布準備恢復招募受試者。
美國媒體報導,嬌生集團首席科學官史托佛(PaulStoffels)表示,試驗暫停期間除公司內部的檢查機制外,還有3個獨立的外部醫學顧問分析問題細節,「沒有發現證據顯示問題與疫苗有關」。
史托佛說,美國的試驗應能在26日前恢復進行,他以隱私為由不透露先前試驗出現副作用的細節,但據華盛頓郵報披露,先前的問題是一名受試者中風。
美國衛生及公共服務部(HHS)官員曼戈(PaulMango)說,他預期美國今年底前就能取得足夠疫苗供「最脆弱」族群,明年1月底前所有年長者都能施打,到明年3、4月底前全體美國民眾都能打得到疫苗。
另一方面,雖然巴西總統波索納洛(JairBolsonaro)本週稍早還宣布不會採購中國北京科興生物公司(Sinovac Biotech)的疫苗Coronavac,但巴西國家衛生監測局(Anvisa)今天中午發表聲明,特許北京科興的研究夥伴、聖保羅的布坦坦研究所(Instituto Butantan)進口600萬劑Coronavac疫苗供第3期臨床試驗之用。
巴西國內為中製疫苗引發爭執,總統嫌棄中製疫苗,但包括聖保羅州長多利亞(Joao Doria)在內的地方首長,以及國會下議院議長梅雅(Rodrigo Maia),都與總統唱反調;多利亞說阻撓北京科興疫苗在巴西的試驗根本就是「犯罪」,痛批總統把疫苗政治化。(譯者:陳怡君/核稿:陳亦偉)1091024