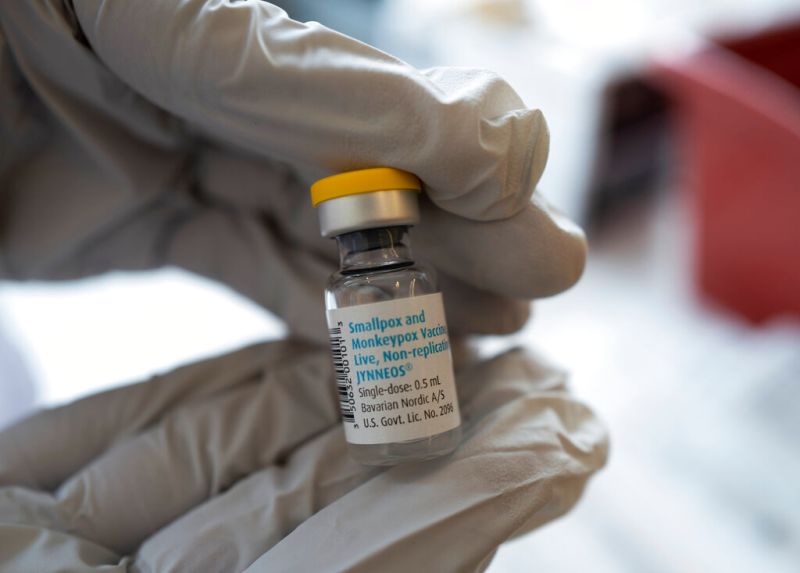
(中央社記者唐雅陵聖保羅19日專電)鑒於世界衛生組織宣布猴痘疫情列為國際公共衛生緊急事件,巴西國家衛生監督局今天一致通過獲特定國際權威監管機構批准的猴痘藥物和疫苗進口豁免註冊。
巴西國家衛生監督局(Anvisa)指出,這項規定為臨時性質,允許巴西衛生部針對已獲特定國際權威監管機構批准用於預防或治療猴痘的藥物和疫苗,向當局申請豁免註冊。
這些機構包括世界衛生組織(WHO)、歐盟藥品管理局(EMA)、美國食品暨藥物管理局(FDA)、英國藥物及保健產品管理局(MHRA)、日本厚生勞動省醫藥品醫療機計綜合機構(PMDA/MHLW)和加拿大衛生署(Health Canada)。
國家衛生監督局長托雷斯(Antonio Barra Torres)指出,豁免註冊是一種監管辦法,不意味默許所有用於預防或治療猴痘的藥物和疫苗。進口藥品或疫苗的所有生產場所,包括生產線和形式都必須經過前述國際監管機構批准。
國家衛生監督局將採取類似通過COVID-19(2019冠狀病毒疾病)疫苗全球取得機制(Covax)的進口模式,由當局的技術部門優先評估豁免註冊的請求,在7個工作日內做出決定。
使用藥物或疫苗的弱勢群體和優先群體將由巴西衛生部決定。衛生部也將負責監督進口藥品或疫苗的使用,向衛生服務部門通報不良反應和技術性投訴。
巴西衛生部將確保藥物或疫苗符合國際監管機構批准的條件,確保疫苗僅在國家衛生質量控制研究所(INCQS)批准後使用。
國家衛生監督局將密切關注與世衛組織和國際監管機構關於藥物警戒和有效性的討論。
根據衛生部,巴西有3450例猴痘確診病例,主要集中在聖保羅州2279例,里約熱內盧州403例,米納斯吉拉斯州(Minas Gerais)159例,以及聯邦特區巴西利亞141例。(編輯:馮昭)1110820
我是廣告 請繼續往下閱讀
這些機構包括世界衛生組織(WHO)、歐盟藥品管理局(EMA)、美國食品暨藥物管理局(FDA)、英國藥物及保健產品管理局(MHRA)、日本厚生勞動省醫藥品醫療機計綜合機構(PMDA/MHLW)和加拿大衛生署(Health Canada)。
國家衛生監督局長托雷斯(Antonio Barra Torres)指出,豁免註冊是一種監管辦法,不意味默許所有用於預防或治療猴痘的藥物和疫苗。進口藥品或疫苗的所有生產場所,包括生產線和形式都必須經過前述國際監管機構批准。
國家衛生監督局將採取類似通過COVID-19(2019冠狀病毒疾病)疫苗全球取得機制(Covax)的進口模式,由當局的技術部門優先評估豁免註冊的請求,在7個工作日內做出決定。
使用藥物或疫苗的弱勢群體和優先群體將由巴西衛生部決定。衛生部也將負責監督進口藥品或疫苗的使用,向衛生服務部門通報不良反應和技術性投訴。
巴西衛生部將確保藥物或疫苗符合國際監管機構批准的條件,確保疫苗僅在國家衛生質量控制研究所(INCQS)批准後使用。
國家衛生監督局將密切關注與世衛組織和國際監管機構關於藥物警戒和有效性的討論。
根據衛生部,巴西有3450例猴痘確診病例,主要集中在聖保羅州2279例,里約熱內盧州403例,米納斯吉拉斯州(Minas Gerais)159例,以及聯邦特區巴西利亞141例。(編輯:馮昭)1110820