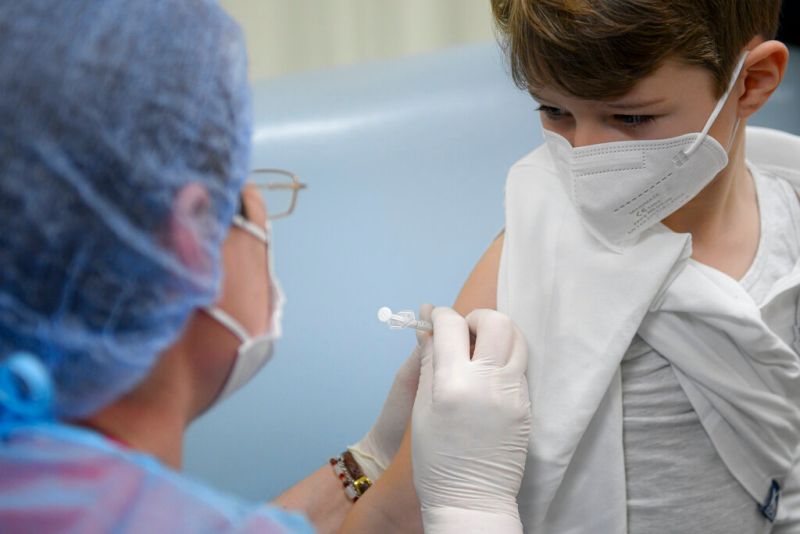
(中央社華盛頓15日綜合外電報導)在美國家長焦急等待之際,食品暨藥物管理局(FDA)專家小組今天召開會議,考慮是否建議為5歲至6個月幼兒接種COVID-19(2019冠狀病毒疾病)疫苗。
在美國和多數其他國家,5歲以下幼兒是唯一尚未獲准接種COVID-19疫苗的年齡組。如果專家小組一如預期投票贊成批准輝瑞(Pfizer)和莫德納(Moderna)疫苗,正式授權將很快跟進,預計下週就可開始接種。
FDA在會議前發布針對這兩種疫苗的獨立分析,並認為它們安全且有效。FDA認為,由於這個年齡組幼兒住院率和死亡率「高於5至17歲兒童和青少年」,因此迫切需要接種疫苗。
目前輝瑞正尋求授權為6個月至4歲幼兒注射3劑3微克疫苗;而莫德納已要求FDA批准為6個月至5歲幼兒注射2劑30微克疫苗。
這兩間藥廠經過試驗後,發現輝瑞疫苗避免幼兒染疫的療效可達80%;而莫德納估計,針對6個月到2歲群組,療效為51%,2至5歲群組則為37%。
這些數據只是初步資料,莫德納正研究第3劑的效果,其保護力數據可能進一步提高。
目前美國約有2000萬名4歲(含)以下兒童。若FDA建議幼兒接種這2種疫苗,接下來將交由美國疾病管制暨預防中心(CDC)做出最終決定。
白宮官員上週表示,可能最早於6月21日開始,就可在藥房或醫療院所施打數以百萬計的幼兒疫苗。(譯者:林沂鋒/核稿:施施)1110615
我是廣告 請繼續往下閱讀
FDA在會議前發布針對這兩種疫苗的獨立分析,並認為它們安全且有效。FDA認為,由於這個年齡組幼兒住院率和死亡率「高於5至17歲兒童和青少年」,因此迫切需要接種疫苗。
目前輝瑞正尋求授權為6個月至4歲幼兒注射3劑3微克疫苗;而莫德納已要求FDA批准為6個月至5歲幼兒注射2劑30微克疫苗。
這兩間藥廠經過試驗後,發現輝瑞疫苗避免幼兒染疫的療效可達80%;而莫德納估計,針對6個月到2歲群組,療效為51%,2至5歲群組則為37%。
這些數據只是初步資料,莫德納正研究第3劑的效果,其保護力數據可能進一步提高。
目前美國約有2000萬名4歲(含)以下兒童。若FDA建議幼兒接種這2種疫苗,接下來將交由美國疾病管制暨預防中心(CDC)做出最終決定。
白宮官員上週表示,可能最早於6月21日開始,就可在藥房或醫療院所施打數以百萬計的幼兒疫苗。(譯者:林沂鋒/核稿:施施)1110615