亞洲國家新冠肺炎(COVID-19)疫情仍然嚴峻,但是國際大廠製造的新冠疫苗仍然供不應求,各國面臨接種壓力,促使台灣、韓國、日本都動用所有資源,希望能儘早開發國產疫苗。韓國已經有數家藥廠可望在今年進入第三期臨床實驗;日本政府祭出至少484億日圓補助,投入國產疫苗研發,不少藥廠也在今年初展開1/2期臨床試驗。
根據《日經亞洲評論》(Nikkei Asia)報導,不少韓國民眾一邊羨慕美國完成接種後不需要戴口罩,一邊批評韓國政府採購疫苗策略以及國產疫苗研發進度緩慢;台灣在本土確診病例激增之後,也面臨了接種壓力;日本因為施打疫苗的進度緩慢而備受批評,一個政府顧問委員會上周便提出一項提案,盼能強化國內開發疫苗的量能。
雖然台灣、韓國、日本都希望能盡快研發出國產疫苗來遏止國內疫情擴散,同時提供國民每年追加接種的疫苗數量,最終力拚出口。然而,這並非容易的事情。衛生當局以及藥廠都表示,可能需要費時數個月、甚至是數年,才能讓企業完成研究,並且取得生產疫苗的許可證。
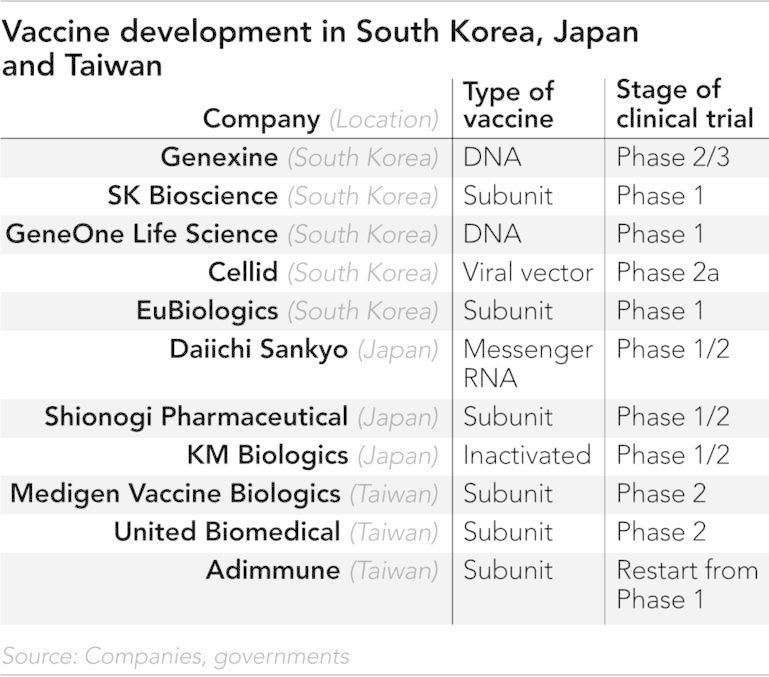
韓國目前有5間生技公司研發疫苗,正在進行第1階段或第2階段的臨床試驗,其中部份公司預計將在今年稍晚進入第3階段。其中進度最快的藥廠Genexine,今年3月為其DNA疫苗GX-19N疫苗,在印尼展開2/3期臨床試驗計畫,將對印尼5家醫院的1千名試驗者施打疫苗。Genexine則是5月稍早,已經在韓國展開2a期臨床試驗,對6家醫院的150受試者施打疫苗。另外SK生物科學公司(SK Bioscience)和GeneOne生命科學公司正分別對次單位疫苗與DNA疫苗,進行第一期試驗。藥廠Cellid也說,其公司的AdCLD疫苗已在5家醫院完成2a期臨床試驗。
藥廠Genexine的執行長Woo Jung-won接受訪問時表示「如果在開發途中放棄,很有可能就沒有面對下一波大流行的選項,企業和政府應盡最大努力完成這次開發疫苗競賽」
而日本也有多達四間公司正在進行疫苗研發,東京的第一三株式會社(Daiichi Sankyo)正研發mRNA疫苗,並在3月開始1/2期臨床試驗;大阪的鹽野義製藥(Shionogi Pharmaceutical)則是採用桿狀病毒和棘蛋白製作疫苗,並也已經在去年12月展開1/2期臨床試驗;KM生技(KM Biologics)正在研發一款傳統的滅活疫苗(inactivated vaccine),也在今年3月開始1/2期試驗。
這四家日本藥廠已共取得至少484億日圓(約122億元台幣)的疫苗研發與生產政府補助金,目前日本政府也正在討論設立研發中心,提高研究投資,加快批准程序。
日本政府討論的方案包括向藥廠採買更多的疫苗,並以更高的定價採買新藥,讓廠商能有更強烈的動機投入研發。因為日本健保體系為單一保險人支付制度,所以藥物的定價基本上是由政府來決定。
報導中提到,台灣目前有高端、聯亞、國光生技3間公司研發國產疫苗,目前高端以及聯亞都已經進入第二期臨床實驗。而高端已經在生產疫苗,一旦獲得美國食品藥物管理局(FDA)的緊急使用授權,該疫苗將能直接使用。