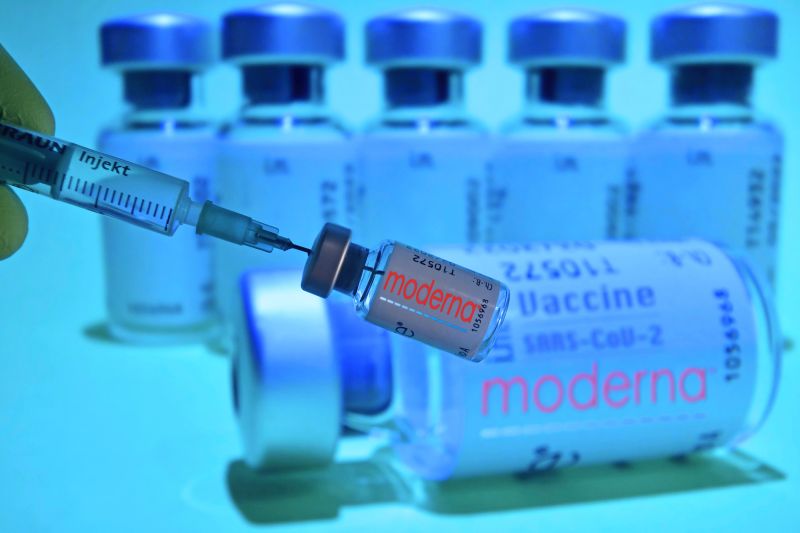
美國新型冠狀病毒(COVID-19)至16日上午累計逾1671萬例,死亡人數突破30萬。日前美國食品藥品監督管理局(FDA)批准藥廠輝瑞(Pfizer)和德國生計BioNTech共同研發的疫苗,並於週一(14)正式開始為民眾接種;同時,FDA指莫德納(Moderna)公司研發的疫苗,保護力達94.1%,且無安全性疑慮,最快將在本週五(18)批准疫苗使用。
據《紐約時報》報導,莫德納11月30日向FDA呈交完整的疫苗試驗數據。FDA於昨日(15)公開數據表示,根據3萬人的臨床實驗結果顯示,莫德納研發的疫苗能夠對病毒形成94.1%的保護力。同時,疫苗的副作用包括:發燒、頭痛、疲倦等,雖然會引起輕微不適但整體沒有危險性。FDA指出,試驗數據符合緊急使用的預期,外部專家會議評估過後,莫德納疫苗有望成為美國FDA第二個批准授權使用的新冠疫苗。
輝瑞疫苗必須儲存在零下70度的環境,藥廠同時開發出內含乾冰的包裝,以延長疫苗儲存時間。莫德納疫苗則需要在零下20度的環境儲存,最長可以保存6個月,在家用冰箱內可以儲存30天,常溫下則是12個小時。兩種疫苗的防護力都約為95%,且需要分2劑接種。
負責監管疫苗分配工作的美國官員表示,莫德納提供的首批疫苗數量將是輝瑞藥廠(290萬劑)的兩倍,將由藥物經銷商負責包裝、分配至各集散點,再由FedEx、UPS貨運公司運送至目的地。美國政府目前已向輝瑞訂購1億劑疫苗,莫德納疫苗獲批准後,預計至12月底美國將有2000萬人接種。
同時,白宮新聞秘書麥肯奈妮(Kayleigh McEnany)15日於新聞發佈會上表示,川普總統將會接種新冠疫苗且態度「絕對地」(absolutely)鼓勵民眾施打。麥肯奈妮表示,總統的醫療團隊評估哪暖疫苗最有效之後,川普將會接種疫苗,同時脆弱的高風險群體是最迫切需要接種的美國人。
※【NOWnews 今日新聞】提醒您:
因應新冠肺炎疫情,疾管署持續加強疫情監測與邊境管制措施,國外入境後如有發燒、咳嗽等不適症狀,請撥打「1922」專線,或「0800-001922」,並依指示配戴口罩儘速就醫,同時主動告知醫師旅遊史及接觸史,以利及時診斷及通報。
我是廣告 請繼續往下閱讀
輝瑞疫苗必須儲存在零下70度的環境,藥廠同時開發出內含乾冰的包裝,以延長疫苗儲存時間。莫德納疫苗則需要在零下20度的環境儲存,最長可以保存6個月,在家用冰箱內可以儲存30天,常溫下則是12個小時。兩種疫苗的防護力都約為95%,且需要分2劑接種。
負責監管疫苗分配工作的美國官員表示,莫德納提供的首批疫苗數量將是輝瑞藥廠(290萬劑)的兩倍,將由藥物經銷商負責包裝、分配至各集散點,再由FedEx、UPS貨運公司運送至目的地。美國政府目前已向輝瑞訂購1億劑疫苗,莫德納疫苗獲批准後,預計至12月底美國將有2000萬人接種。
同時,白宮新聞秘書麥肯奈妮(Kayleigh McEnany)15日於新聞發佈會上表示,川普總統將會接種新冠疫苗且態度「絕對地」(absolutely)鼓勵民眾施打。麥肯奈妮表示,總統的醫療團隊評估哪暖疫苗最有效之後,川普將會接種疫苗,同時脆弱的高風險群體是最迫切需要接種的美國人。
※【NOWnews 今日新聞】提醒您:
因應新冠肺炎疫情,疾管署持續加強疫情監測與邊境管制措施,國外入境後如有發燒、咳嗽等不適症狀,請撥打「1922」專線,或「0800-001922」,並依指示配戴口罩儘速就醫,同時主動告知醫師旅遊史及接觸史,以利及時診斷及通報。