我是廣告 請繼續往下閱讀
食藥署指出,截至昨日止,經確認市售含 ranitidine 成分藥品共 15 項、 287 批,已提出檢驗合格證明文件,得恢復供應、銷售;另共 23 項、 420 批藥品應啟動回收作業,並應於 11 月 18 日前完成回收。
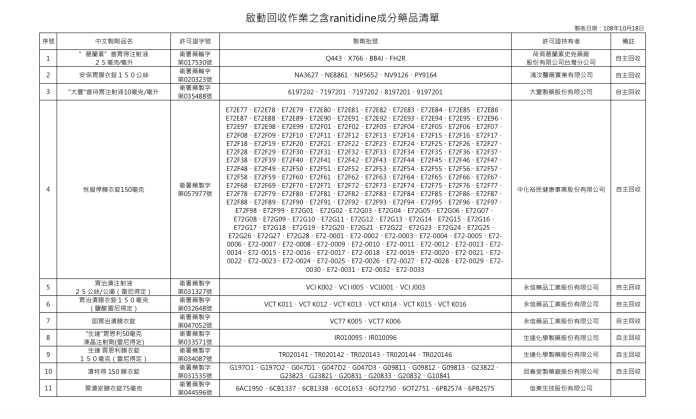 ▲共 23 項、 420 批藥品應啟動回收作業。(圖/食藥署)
▲共 23 項、 420 批藥品應啟動回收作業。(圖/食藥署)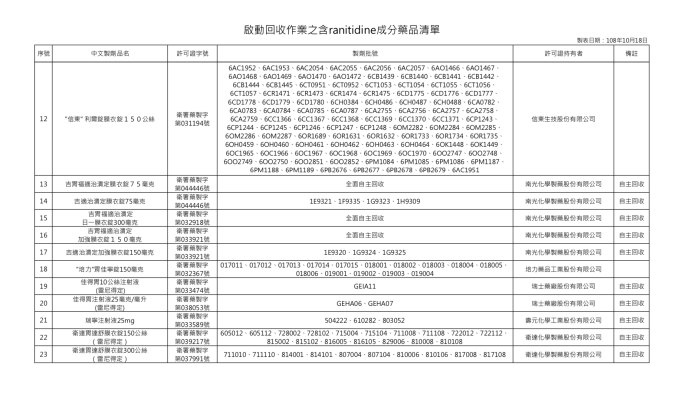 ▲共 23 項、 420 批藥品應啟動回收作業。(圖/食藥署)
▲共 23 項、 420 批藥品應啟動回收作業。(圖/食藥署)食藥署強調, NDMA 成分雖具動物致癌性,然對人類資料尚未證明,正在服用之民眾,切勿隨意自行停藥,以免影響疾病治療,應儘速回診,與醫師或藥師討論,處方其他適當藥品。
食藥署說,為確保 ranitidine 藥品品質,已採取風險管理措施,要求相關業者暫停輸入、供應 ranitidine 原料藥,並應提出預防矯正措施,且應逐批檢驗原料藥是否含有 NDMA ,經確認檢驗合格後,始得供製造使用,後續將對進行上市後藥品品質安全監控。


